KIMIA
Molalitas dan Fraksi Mol
Dalam larutan, terdapat beberapa sifat zat yang hanya ditentukan oleh banyaknya partikel zat terlarut
[2]. Oleh karena sifat koligatif larutan ditentukan oleh banyaknya partikel zat terlarut, maka perlu diketahui tentang
konsentrasi larutan[2].
Molalitas (m)
Molalitas (kemolalan) adalah jumlah
mol zat terlarut dalam 1 kg (1000 gram) pelarut
[2]. Molalitas didefinisikan dengan persamaan berikut
[2]:
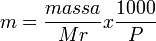
m = molalitas larutan (mol / kg)
n = jumlah mol zat terlarut (g / mol)
P = massa pelarut (g)
Fraksi Mol
Fraksi mol merupakan satuan konsentrasi yang semua komponen larutannya dinyatakan berdasarkan mol
[2]. Fraksi mol komponen

, dilambangkan dengan

adalah jumlah mol komponen

dibagi dengan jumlah mol semua komponen dalam larutan
[2]. Fraksi mol

adalah

dan seterusnya
[2]. Jumlah fraksi mol dari semua komponen adalah 1
[2]. Persamaannya dapat ditulis
[2]. Molalitas didefinisikan dengan persamaan berikut
[2]
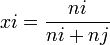
Sifat Koligatif Larutan Nonelektrolit
Meskipun sifat koligatif melibatkan larutan, sifat koligatif tidak
bergantung pada interaksi antara molekul pelarut dan zat terlarut,
tetapi bergatung pada jumlah zat terlarut yang larut pada suatu larutan
[3]. Sifat koligatif terdiri dari penurunan tekanan uap, kenaikan titik didih, penurunan titik beku, dan tekanan osmotik
[3].
Penurunan Tekanan Uap

Marie Francois Raoult (1830 – 1901) ilmuwan yang menyimpulkan tentang tekanan uap jenuh larutan
Molekul – molekul zat cair yang meninggalkan permukaan menyebabkan adanya tekanan
uap zat cair[3]. Semakin mudah molekul – molekul zat cair berubah menjadi uap, makin tinggi pula tekanan uapzat cair
[3].
Apabila tekanan zat cair tersebut dilarutkan oleh zat terlarut yang
tidak menguap, maka partikel – partikel zat terlarut ini akan mengurangi
penguapan molekul – molekul zat cair
[3].
Laut mati adalah contoh dari terjadinya penurunan tekanan uap pelarut oleh zat terlarut yang tidak mudah menguap.
Air berkadar
garam sangat tinggi ini terletak di daerah
gurun yang sangat panas dan kering, serta tidak berhubungan dengan
laut bebas, sehingga konsentrasi zat terlarutnya semakin tinggi
[3]. Persamaan penurunan tekanan uap dapat ditulis
[3] :

P
0 – P
P
0 > P
P
0 = tekanan uap zat cair murni
P = tekanan uap larutan
Pada tahun 1808, Marie Francois Raoult seorang
kimiawan asal
Perancis
melakukan percobaan mengenai tekanan uap jenuh larutan, sehingga ia
menyimpulkan tekanan uap jenuh larutan sama dengan fraksi mol pelarut
dikalikan dengan tekanan uap jenuh pelarut murni
[3]. Persamaan penurunan tekanan uap dapat ditulis
[3]. Kesimpulan ini dikenal dengan
Hukum Raoult dan dirumuskan dengan
[3]. Persamaan penurunan tekanan uap dapat ditulis
[3] :
P = P
0 x Xp

= P
0 x Xt
P = tekanan uap jenuh larutan
P
0 = tekanan uap jenuh pelarut murni
Xp = fraksi mol zat pelarut
Xt = fraksi mol zat terlarut

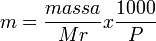
 , dilambangkan dengan
, dilambangkan dengan  adalah jumlah mol komponen
adalah jumlah mol komponen  adalah
adalah  dan seterusnya
dan seterusnya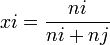

 P0 – P
P0 > P
P0 – P
P0 > P = P0 x Xt
= P0 x Xt